
- Հեղինակ Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Վերջին փոփոխված 2025-06-01 05:04.
Քլորը իզոտոպ 18 նեյտրոններով ունի 0,7577 առատություն և 35 ամու զանգվածային թիվը։ Հաշվարկելու համար միջին ատոմային զանգված, յուրաքանչյուրի համար կոտորակը բազմապատկեք զանգվածային թվով իզոտոպ , ապա դրանք միասին ավելացրեք։
Նմանապես, ո՞րն է տարրի բոլոր իզոտոպների կշռված միջինը:
Օգտագործելով տարբեր զանգվածները իզոտոպներ և որքան առատ է յուրաքանչյուրը իզոտոպ այսինքն, մենք կարող ենք գտնել միջին ան-ի ատոմների զանգվածը տարր . Ան-ի ատոմային զանգվածը տարր է կշռված միջին ատոմների զանգվածը բնական նմուշում տարր . Ատոմային զանգվածը սովորաբար հաղորդվում է ատոմային զանգվածի միավորներով:
Որքա՞ն է 1 ամու զանգվածը: Ատոմային զանգվածի միավորը (խորհրդանշվում է AMU կամ amu) սահմանվում է որպես ածխածնի 12 ատոմի զանգվածի ճշգրիտ 1/12: Ածխածնի-12 (C-12) ատոմն ունի վեց պրոտոններ և վեց նեյտրոններ իր միջուկում։ Անճշգրիտ առումով, մեկ AMU-ն միջինն է պրոտոն հանգստի զանգվածը և նեյտրոն հանգստի զանգված.
Երկրորդ, ինչպե՞ս եք հաշվարկում տոկոսային առատությունը՝ օգտագործելով ատոմային զանգվածը:
Փոխեք յուրաքանչյուրը տոկոս առատություն տասնորդական ձևի` բաժանելով 100-ի: Այս արժեքը բազմապատկեք ատոմային զանգված այդ իզոտոպից։ Յուրաքանչյուր իզոտոպի համար գումարեք՝ միջինը ստանալու համար ատոմային զանգված.
Ո՞րն է տարբերությունը ատոմային զանգվածի և ատոմային քաշի միջև:
Ատոմային զանգված (մա) է զանգվածային ան ատոմ . Մի սինգլ ատոմ ունի պրոտոնների և նեյտրոնների որոշակի քանակ, ուստի զանգվածային միանշանակ է (չի փոխվի) և պրոտոնների և նեյտրոնների քանակի գումարն է ատոմում . Ատոմային քաշը -ի կշռված միջինն է զանգվածային բոլորից ատոմներ տարրի՝ հիմնված իզոտոպների առատության վրա։
Խորհուրդ ենք տալիս:
Ինչպե՞ս կարելի է գտնել հեղուկ խառնուրդի տեսակարար կշիռը:

Այժմ բաժանեք ընդհանուր խտությունը ջրի խտության վրա և կստանաք խառնուրդի SG: Ո՞րն է ամենաբարձր խտությամբ հեղուկը: Երբ երկու նյութերի հավասար ծավալը խառնվում են, խառնուրդի տեսակարար կշիռը 4 է։ P խտությամբ հեղուկի զանգվածը խառնվում է 3p խտությամբ մեկ այլ հեղուկի անհավասար զանգվածի հետ։
Ինչպե՞ս կարելի է գտնել կենտրոնական անկյունը՝ հաշվի առնելով հատվածի մակերեսը և շառավիղը:

Կենտրոնական անկյունի որոշումը հատվածի տարածքից (πr2) × (կենտրոնական անկյունը ÷ 360 աստիճանով) = հատվածի տարածքը: Եթե կենտրոնական անկյունը չափվում է ռադիաններով, ապա բանաձևը դառնում է սեկտորի տարածք = r2 × (կենտրոնական անկյունը ռադիաններով ÷ 2): (θ ÷ 360 աստիճան) × πr2. (52,3 ÷ 100π) × 360. (52,3 ÷ 314) × 360
Ինչպե՞ս գտնել բաց թողնված թիվը, երբ տրվում է միջինը:

Թվերի բազմության միջինը այդ թվերի միջինն է: Դուք կարող եք գտնել թեման՝ ավելացնելով թվերի բազմությունը և բաժանելով քանի թվերի տրված: Եթե ձեզ տրված է թեմա և խնդրել են գտնել բաց թողնված թիվ այս շարքից, օգտագործեք պարզ հավասարում
Ինչպե՞ս եք ստեղծում կշռված միջինը առանցքային աղյուսակում:

Կշռված միջինները առանցքային աղյուսակում Սեղմեք PivotTable-ի գործիքագոտու ձախ կողմում գտնվող PivotTable բառի կողքին գտնվող ներքև սլաքը: Ընտրեք բանաձևեր | Հաշվարկված դաշտեր. Անուն վանդակում մուտքագրեք անուն ձեր նոր դաշտի համար: Բանաձևի դաշտում մուտքագրեք բանաձևը, որը ցանկանում եք օգտագործել ձեր միջին կշռված համար, օրինակ՝ =WeightedValue/Weight: Սեղմեք OK
Ինչպե՞ս գտնել միջինը Excel-ի միջոցով:
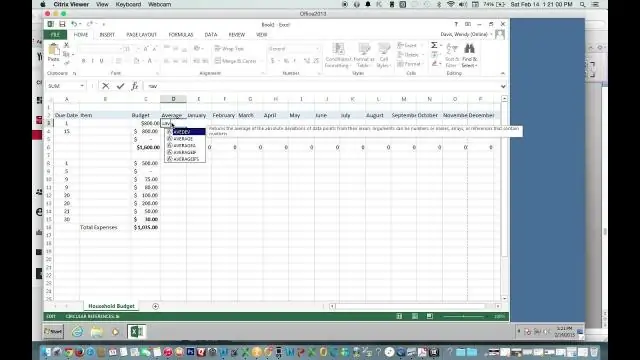
Օգտագործեք AutoSum՝ միջինը արագ գտնելու համար Սեղմեք սյունակի տակ գտնվող բջիջի վրա կամ այն թվերի տողից աջ, որոնց համար ցանկանում եք գտնել միջինը: HOME ներդիրում սեղմեք AutoSum > Average-ի կողքին գտնվող սլաքը, այնուհետև սեղմեք Enter
