
- Հեղինակ Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Վերջին փոփոխված 2025-01-22 17:00.
(1), (3) H2O և NH3 մոլեկուլներ են, որոնք պարունակում են բևեռ կովալենտային կապեր , բայց դրանց էլեկտրոնների բաշխումը սիմետրիկ չէ։ (4) H2-ը ոչ բևեռային մոլեկուլ է, որն ունի էլեկտրոնների սիմետրիկ բաշխում, սակայն ջրածնի ատոմների միջև կապը ոչ բևեռային կովալենտ է։
Հետևաբար, ո՞ր բանաձևն է ներկայացնում ոչ բևեռ մոլեկուլները:
Ա) H2O Բ) Ո՞ր բանաձևն է ներկայացնում բևեռ պարունակող ոչ բևեռային մոլեկուլ կովալենտային կապեր ?
Բացի այդ, ո՞ր մոլեկուլներն էին ոչ բևեռ, քանի որ բոլոր կապերը ոչ բևեռ էին: Եւ մոլեկուլները որ ոչ բևեռ են, քանի որ բոլոր պարտատոմսերը ոչ բևեռ են Ջրածին (H2), քլոր (Cl2), ազոտ (N2) և թթվածին (O2) բոլորը ոչ բևեռ են, քանի որ նրանք են նույն տեսակի տարրերը և երկուսն էլ ունեն նույն թվով էլեկտրաբացասականություն:
Բացի այդ, ինչպե՞ս կարող է մոլեկուլը լինել ոչ բևեռ, եթե այն պարունակում է բևեռային կապեր։
Ա մոլեկուլը կարող է տիրապետել բևեռային կապեր և դեռ լինել ոչ բևեռային . Եթե որ բևեռային կապեր հավասարաչափ (կամ սիմետրիկ) բաշխված են պարտատոմս դիպոլները ջնջում են և չեն ստեղծում ա մոլեկուլային դիպոլ.
Ո՞ր մոլեկուլն է ոչ բևեռ.
Ոչ բևեռային մոլեկուլների օրինակներ Համասեռամիջուկային ոչ բևեռ մոլեկուլների օրինակներ են թթվածինը (O2), ազոտ (N2), և օզոն (Օ3) Այլ ոչ բևեռ մոլեկուլները ներառում են ածխաթթու գազ ( CO2 ) և մեթանի օրգանական մոլեկուլները ( Չ4 ), տոլուոլ և բենզին։ Ածխածնի միացությունների մեծ մասը ոչ բևեռ է: Հատկանշական բացառություն է ածխածնի երկօքսիդը, CO:
Խորհուրդ ենք տալիս:
Արդյո՞ք բևեռային մոլեկուլները վանում են ոչ բևեռային մոլեկուլները:

Բևեռային մոլեկուլները (+/- լիցքերով) ձգվում են դեպի ջրի մոլեկուլները և հիդրոֆիլ են։ Ոչ բևեռային մոլեկուլները վանվում են ջրով և չեն լուծվում ջրի մեջ. հիդրոֆոբ են
Պարտատոմսերը բևեռային են, թե ոչ բևեռային:

ԲԵՎԵՌ ԵՎ ՈՉ ԲԵՎԵՌ ՄԻԱՑՈՒԹՅՈՒՆՆԵՐ Մասամբ իոնային կապերը կոչվում են բևեռային կովալենտային կապեր։ Ոչ բևեռային կովալենտային կապերը, որոնք ունեն կապի էլեկտրոնների հավասար բաշխում, առաջանում են, երբ երկու ատոմների էլեկտրաբացասականությունը հավասար են։ Արդյունքը կապ է, որտեղ էլեկտրոնային զույգը տեղաշարժվում է դեպի ավելի էլեկտրաբացասական ատոմ
Cl Cl-ը բևեռային է, թե ոչ բևեռային:

Երբ տարբերությունը շատ փոքր է կամ զրո, կապը կովալենտ է և ոչ բևեռ: Երբ այն մեծ է, կապը բևեռային կովալենտ է կամ իոնային: H–H, H–Cl և Na–Cl կապերում ատոմների էլեկտրաբացասականության տարբերությունների բացարձակ արժեքները համապատասխանաբար 0 (ոչ բևեռ), 0.9 (բևեռային կովալենտ) և 2.1 (իոնային) են։
Ինչպե՞ս գրել բազմատոմ իոն պարունակող միացության բանաձևը:
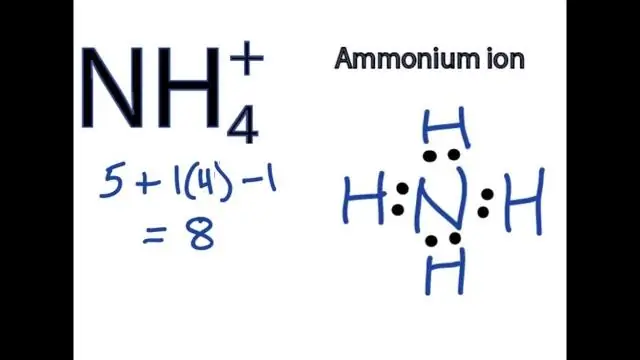
Բազմանատոմային իոններ պարունակող միացությունների բանաձևեր գրելու համար գրեք մետաղական իոնի խորհրդանիշը, որին հաջորդում է բազմատոմիոնի բանաձևը և հավասարակշռեք լիցքերը: Բազմանատոմ իոն պարունակող միացությունը անվանելու համար նախ նշեք կատիոնը, ապա անիոնը
Օզոնն ունի՞ բևեռային կապեր:

Ավելի մեծ մոլեկուլները, նույնիսկ եթե ունեն միայն մեկ տեսակի ատոմ, երբեմն բևեռային են: Դա տեղի կունենա, երբ կենտրոնական ատոմն ունի մեկ կամ մի քանի զույգ ոչ կապող դելեկտրոններ: Դրա օրինակներից է օզոնը՝ O3-ը: Թթվածնի միջին ատոմն ունի էլեկտրոնների միայնակ զույգ, և այս զույգը մոլեկուլին տալիս է իր բևեռականությունը
