
- Հեղինակ Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Վերջին փոփոխված 2025-06-01 05:04.
E1 ցույց է տալիս Ա վերացում , միամոլեկուլային ռեակցիա , որտեղ տոկոսադրույքը = k [R-LG]: Ան-ում E1 ռեակցիա , է տոկոսադրույքը որոշիչ քայլը հեռացող խմբի կորուստն է՝ միջանկյալ կարբոկատիոն ձևավորելու համար: Որքան ավելի կայուն է կարբոկատիոնը, այնքան ավելի հեշտ է այն ձևավորվում և ավելի արագ E1 ռեակցիա կլինի.
Պարզապես, ինչպե՞ս եք անում e1 ռեակցիան:
Ան E1 ռեակցիա ներառում է ջրածնի ապապրոտոնացում մոտակայքում (սովորաբար մեկ ածխածնի հեռավորության վրա, կամ բետա դիրքում) կարբոկացիան, որի արդյունքում առաջանում է ալկենի արտադրանք: Դա անելու համար անհրաժեշտ է Լյուիսի բազա:
Բացի այդ, ո՞րն է տարբերությունը e1 և e2 ռեակցիաների միջև: Մեխանիկորեն, E2 ռեակցիաներ համաձայնեցված են (և առաջանում են ավելի արագ), մինչդեռ E1 ռեակցիաներ աստիճանաբար են (և առաջանում են ավելի դանդաղ և ավելի բարձր էներգիայի ծախսերով, ընդհանուր առմամբ): Շնորհիվ E1-ները մեխանիկական վարքագիծը, կարբոկացիոն վերադասավորումները կարող են առաջանալ մեջ միջանկյալ, այնպիսին, որ դրական լիցքը տեղափոխվում է ամենակայուն ածխածնի վրա:
Հաշվի առնելով սա, ո՞րն է e2 ռեակցիայի արագության հավասարումը:
E2 ցույց է տալիս ան վերացում , երկմոլեկուլային ռեակցիա , որտեղ տոկոսադրույքը = k [B][R-LG]: Ան-ում E2 ռեակցիա , է ռեակցիա փոխակերպում է 2 sp3 C ատոմների մեջ sp2 C ատոմներ. Սա տեղափոխում է փոխարինողներն իրարից ավելի հեռու՝ նվազեցնելով ստերիկ փոխազդեցությունները: Այսպիսով, ավելի շատ բարձր փոխարինված համակարգեր են ենթարկվում E2 վերացումն ավելի արագ:
Արդյո՞ք e1 արձագանքը համաձայնեցված է:
Հետևաբար, որքան ավելի կայուն է այդ կարբոկացիան, այնքան ավելի արագ է ռեակցիա կլինի. E2-ի դրույքաչափը ռեակցիա կախված է և՛ սուբստրատից, և՛ հիմքից, քանի որ արագությունը որոշող քայլը երկմոլեկուլային է ( համաձայնեցված ) Ընդհանրապես պահանջվում է ամուր հիմք, որը թույլ կտա տեղաշարժել բևեռային հեռացող խումբը:
Խորհուրդ ենք տալիս:
Ի՞նչ կապ կա ֆերմենտի կոնցենտրացիայի և ռեակցիայի արագության միջև:

Ֆերմենտի կոնցենտրացիան մեծացնելով, ռեակցիայի առավելագույն արագությունը մեծապես մեծանում է: Եզրակացություններ. Քիմիական ռեակցիայի արագությունը մեծանում է, քանի որ սուբստրատի կոնցենտրացիան մեծանում է: Ֆերմենտները կարող են զգալիորեն արագացնել ռեակցիայի արագությունը: Այնուամենայնիվ, ֆերմենտները դառնում են հագեցած, երբ սուբստրատի կոնցենտրացիան բարձր է
Ո՞րն է տարբերությունը շրջակա միջավայրի բացթողման արագության և ադիաբատիկ բացթողման արագության միջև:
Ա. Շրջակա միջավայրի անկման արագությունը վերաբերում է տրոպոսֆերայում բարձրության բարձրացման հետ կապված ջերմաստիճանի անկմանը. դա շրջակա միջավայրի ջերմաստիճանն է տարբեր բարձրությունների վրա: Դա ենթադրում է օդի շարժի բացակայություն։ Ադիաբատիկ սառեցումը կապված է միայն բարձրացող օդի հետ, որը սառչում է ընդարձակմամբ
Որո՞նք են արագության և արագության զգալի նմանություններն ու տարբերությունները:
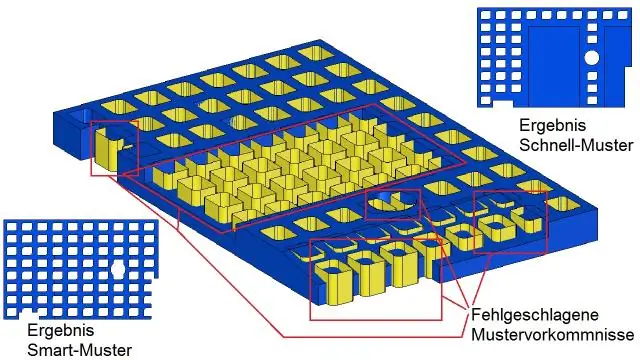
Համեմատության գծապատկեր Համեմատության արագության արագության հիմքը Հեռավորության փոփոխության արագությունը Տեղաշարժի փոփոխություն Երբ մարմինը վերադառնում է իր սկզբնական դիրքին Չի լինի զրո Չի լինի զրո Շարժվող օբյեկտի արագությունը երբեք չի կարող բացասական լինել: Շարժվող օբյեկտի արագությունը կարող է լինել դրական, բացասական կամ զրո
Ո՞րն է տարբերությունը արագության և արագության միջև օրինակներով:
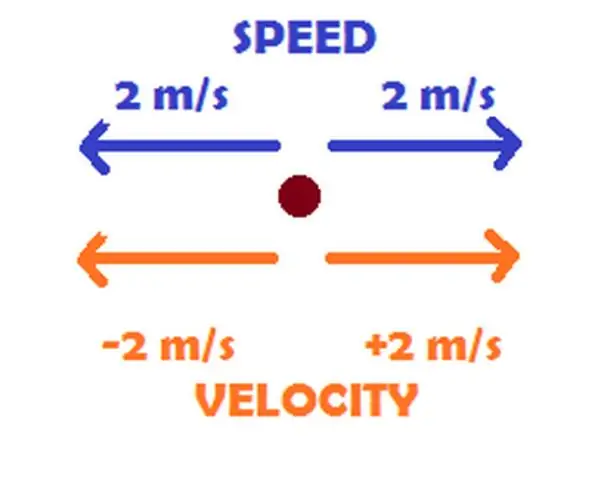
Պատճառը պարզ է. Արագությունը ժամանակի արագությունն է, երբ օբյեկտը շարժվում է ուղու երկայնքով, մինչդեռ արագությունը օբյեկտի շարժման արագությունն ու ուղղությունն է: Օրինակ՝ 50 կմ/ժ (31 մղոն/ժ) նկարագրում է այն արագությունը, որով մեքենան շարժվում է ճանապարհի երկայնքով, մինչդեռ 50 կմ/ժ արևմուտքը նկարագրում է այն արագությունը, որով նա շարժվում է։
Ո՞րն է տարբերությունը ակնթարթային և միջին արագության միջև, որն է ակնթարթային արագության ամենամեծ օրինակը:

Միջին արագությունը ժամանակի ընթացքում միջինացված արագությունն է: Ակնթարթային արագությունը կլինի ցանկացած ակնթարթային արագություն այդ ժամանակահատվածում, որը չափվում է իրական ժամանակի արագաչափով
