
- Հեղինակ Miles Stephen stephen@answers-science.com.
- Public 2024-01-18 08:16.
- Վերջին փոփոխված 2025-01-22 17:01.
- Ոչ ոքի միջուկը։
- Գրի՛ր միջուկում նեյտրոնների և պրոտոնների քանակը։
- Ոչ ոքի առաջին էներգիայի մակարդակը.
- Ոչ ոքի էլեկտրոնները էներգիայի մակարդակներում՝ համաձայն ստորև նշված կանոնների.
- Հետևեք, թե քանի էլեկտրոն է դրված յուրաքանչյուր մակարդակում և էլեկտրոնների քանակը, որոնք մնացել են օգտագործելու համար:
Հաշվի առնելով դա՝ ինչպե՞ս են աշխատում Բորի դիագրամները:
Բորի դիագրամներ ցույց տվեք էլեկտրոնները, որոնք պտտվում են ատոմի միջուկի շուրջ, ինչ-որ չափով նման մոլորակների, որոնք պտտվում են Արեգակի շուրջը: Մեջ Բորի մոդելը , էլեկտրոնները պատկերված են շրջանագծով շարժվող տարբեր թաղանթների վրա՝ կախված նրանից, թե որ տարրն ունեք։ Յուրաքանչյուր շերտ կարող է պահել միայն որոշակի քանակությամբ էլեկտրոններ:
Նմանապես, քանի՞ էլեկտրոն կա շերտում: Յուրաքանչյուր թաղանթ կարող է պարունակել միայն ֆիքսված թվով էլեկտրոններ: Առաջին թաղանթը կարող է պահել մինչև երկու էլեկտրոն , երկրորդ թաղանթը կարող է պահել մինչև ութ (2 + 6) էլեկտրոն, երրորդը կարող է պահել մինչև 18 (2 + 6 + 10) և այլն: Ընդհանուր բանաձևն այն է, որ n-րդ կեղևը սկզբունքորեն կարող է պահել մինչև 2 (n2) էլեկտրոններ.
Համապատասխանաբար, ի՞նչ է Բորի դիագրամը:
Բորի դիագրամը ատոմի պարզեցված տեսողական ներկայացում է, որը մշակվել է դանիացի ֆիզիկոս Նիլս Բորի կողմից 1913 թվականին: Դիագրամը պատկերում է ատոմը որպես դրական լիցքավորված ատոմ: միջուկ շրջապատված է էլեկտրոններ որոնք շրջում են շրջանաձև ուղեծրերով միջուկ էներգիայի դիսկրետ մակարդակներում:
Ինչպե՞ս եք կարդում Բորի մոդելը:
- Նկարի՛ր միջուկը։
- Գրի՛ր միջուկում նեյտրոնների և պրոտոնների քանակը։
- Նկարեք առաջին էներգիայի մակարդակը:
- Էներգետիկ մակարդակներում գծե՛ք էլեկտրոնները ստորև նշված կանոնների համաձայն:
- Հետևեք, թե քանի էլեկտրոն է դրված յուրաքանչյուր մակարդակում և էլեկտրոնների քանակը, որոնք մնացել են օգտագործելու համար:
Խորհուրդ ենք տալիս:
Ինչպե՞ս է կոչվում Ռադերֆորդի ատոմային մոդելը:

Ռադերֆորդի ատոմային մոդելը հայտնի դարձավ որպես միջուկային մոդել։ Միջուկային ատոմում պրոտոններն ու նեյտրոնները, որոնք կազմում են ատոմի գրեթե ողջ զանգվածը, գտնվում են ատոմի կենտրոնում գտնվող միջուկում։ Էլեկտրոնները բաշխված են միջուկի շուրջ և զբաղեցնում են ատոմի ծավալի մեծ մասը
Քանի՞ աղեղ կարելի է գծել շրջանագծի մեջ:
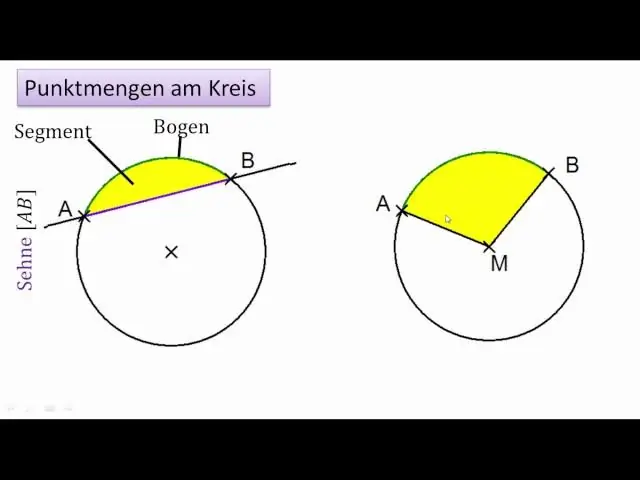
Շրջանակի տրամագիծը այն բաժանում է երկու հավասար աղեղների։ Աղեղներից յուրաքանչյուրը հայտնի է որպես կիսաշրջան: Այսպիսով, ամբողջ շրջանով կա երկու կիսաշրջան: Կիսաշրջաններից յուրաքանչյուրի աստիճանի չափը 180 աստիճան է
Ինչպե՞ս է Բորը փոփոխում Ռադերֆորդի մոդելը:

Կայունության խնդիրը շտկելու համար Բորը փոփոխեց Ռադերֆորդի մոդելը՝ պահանջելով, որ էլեկտրոնները շարժվեն ֆիքսված չափի և էներգիայի ուղեծրերով։ Էլեկտրոնի էներգիան կախված է ուղեծրի չափից և ավելի փոքր ուղեծրերի դեպքում։ Ճառագայթումը կարող է առաջանալ միայն այն ժամանակ, երբ էլեկտրոնը ցատկում է մի ուղեծրից մյուսը
Ինչպե՞ս գծել կովալենտային միացության Լյուիսի կառուցվածքը:

Գծի՛ր մոլեկուլի առանձին ատոմների Լյուիսի խորհրդանիշները: Ատոմները միացրեք այնպես, որ հնարավորության դեպքում յուրաքանչյուր ատոմի շուրջը տեղադրի ութ էլեկտրոն (կամ երկու էլեկտրոն H-ի համար, ջրածին): Ընդհանուր էլեկտրոնների յուրաքանչյուր զույգ կովալենտային կապ է, որը կարող է ներկայացվել գծիկով
Ինչպե՞ս Ռադերֆորդի փորձը հերքեց ատոմի Թոմսոնի մոդելը:

Նա պնդում էր, որ սալորի պուդինգի մոդելը ճիշտ չէ: Լիցքի սիմետրիկ բաշխումը թույլ կտա բոլոր α մասնիկներին անցնել առանց շեղումների։ Ռադերֆորդն առաջարկեց, որ ատոմը հիմնականում դատարկ տարածություն է: Էլեկտրոնները պտտվում են շրջանաձև ուղեծրերով՝ կենտրոնում զանգվածային դրական լիցքի շուրջ
