
- Հեղինակ Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Վերջին փոփոխված 2025-01-22 17:01.
Այսպիսով, ցանկացած էլեկտրոնի կոնֆիգուրացիա որի մեջ որ վերջին էլեկտրոն (կրկին, որ վալենտություն էլեկտրոն ) մեջ է ա ավելի բարձր էներգիայի ուղեծրում, այս տարրն ասում են, որ գտնվում է ան հուզված վիճակ . Օրինակ, եթե նայենք հիմնական վիճակը ( էլեկտրոններ մեջ որ Էներգետիկորեն հասանելի ամենացածր ուղեծրը) թթվածնի, էլեկտրոնի կոնֆիգուրացիան 1s22s22p4 է:
Նաև գիտեք, թե ինչ է դա նշանակում էլեկտրոնների հիմնական վիճակի կոնֆիգուրացիա ասելով:
Այն Էլեկտրոնների հիմնական վիճակի կոնֆիգուրացիա -ի դասավորությունն է էլեկտրոններ էներգիայի ավելի ցածր մակարդակ ունեցող ատոմի միջուկի շուրջ: Այն էլեկտրոններ էներգիայի տարբեր մակարդակների ուղեծրերը զբաղեցնելը, բնականաբար, ընկնում է դեպի ամենացածր էներգիան պետություն կամ հիմնային վիճակ.
Բացի վերևից, ինչպիսի՞ն է Mn ատոմի էլեկտրոնային կոնֆիգուրացիան հիմնական վիճակում: Այն Էլեկտրոնների հիմնական վիճակի կոնֆիգուրացիա -ից հիմնային վիճակ գազային չեզոք մանգան է [Ար]։ 3d5. 4 վրկ2 իսկ տերմինը խորհրդանիշ է 6Ս5/2.
Դրանցից ո՞ր մեկն է գտնվում հիմնական վիճակի կազմաձևում:
Ա գետնին - պետություն Ատոմը ատոմ է, որտեղ էլեկտրոնների ընդհանուր էներգիան չի կարող իջեցվել փոխանցման միջոցով մեկ կամ ավելի շատ էլեկտրոններ տարբեր ուղեծրեր: Այսինքն՝ ա գետնին - պետություն ատոմ, բոլոր էլեկտրոնները գտնվում են էներգիայի հնարավոր ամենացածր մակարդակներում: Օրինակ՝ Դիտարկենք ածխածնի ատոմ, որի էլեկտրոնի կոնֆիգուրացիա հետեւյալն է.
Ի՞նչ է Հունդի կանոնը:
Հունդի կանոն . Հունդի կանոն Ենթափեղանի յուրաքանչյուր ուղեծիր զբաղված է մեկ էլեկտրոնով, նախքան որևէ ուղեծրի կրկնակի զբաղեցում, և առանձին զբաղեցրած ուղեծրերի բոլոր էլեկտրոններն ունեն նույն սպինը:
Խորհուրդ ենք տալիս:
Ո՞րն է քլորի էլեկտրոնային կոնֆիգուրացիան գրգռված վիճակում:

Ո՞ր էլեկտրոնային կոնֆիգուրացիան է ներկայացնում քլորի ատոմը գրգռված վիճակում: (2) 2-8-6-1 սա քլորի գրգռված վիճակն է, պարբերական աղյուսակում հիմնական վիճակը 2-8-7 է: Գրգռված վիճակի էլեկտրոնի կոնֆիգուրացիան ցույց է տալիս էլեկտրոնը, որը թողնում է մեկ էներգիայի մակարդակ և շարժվում դեպի ավելի բարձր մակարդակ
Ո՞րն է SPD և F բլոկի տարրերի ընդհանուր էլեկտրոնային կոնֆիգուրացիան:

Գրեք s-, p-, d- և f- բլոկի տարրերի ընդհանուր արտաքին էլեկտրոնային կոնֆիգուրացիան: Տարր Ընդհանուր արտաքին էլեկտրոնային կոնֆիգուրացիա p–բլոկ (մետաղներ և ոչ մետաղներ) ns2np1–6, որտեղ n = 2 – 6 d–բլոկ (անցումային տարրեր) (n–1) d1–10 ns0–2, որտեղ n = 4 – 7 f –բլոկ(ներքին անցումային տարրեր) (n–2)f1–14(n–1)d0–10ns2, որտեղ n = 6 – 7
Ինչպե՞ս է էլեկտրոնային կոնֆիգուրացիան կապված քվանտային թվերի հետ:
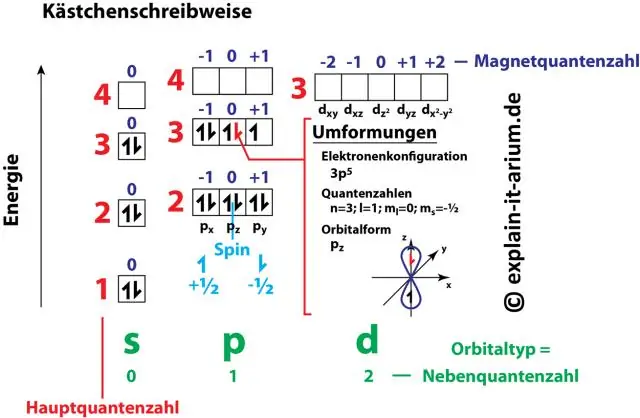
Էլեկտրոնային կոնֆիգուրացիայի մեջ թվերի և տառերի զույգերը ներկայացնում են էլեկտրոնի չորս քվանտային թվերից երկուսը: Այս քվանտային թվերը մեզ ավելի շատ տեղեկություններ են տալիս էլեկտրոնների և նրանց ուղեծրերի հատկությունների մասին: Հիմնական քվանտային թիվը (n) ցույց է տալիս էլեկտրոնի էներգիայի մակարդակը և չափը
Ո՞ր տարրն ունի էլեկտրոնային կոնֆիգուրացիան 2 5:

ՆԿԱՐ 5.9 Սլաքը ցույց է տալիս ենթամակարդակների լրացման հերթականությունը հիշելու երկրորդ եղանակը: Աղյուսակ 5.2-ում ներկայացված են 1-ից 18 ատոմային թվերով տարրերի էլեկտրոնային կոնֆիգուրացիաները: Տարր Ատոմային թիվ Էլեկտրոնի կոնֆիգուրացիա ծծումբ 16 1s22s22p63s23p4 քլոր 17 1s22s22p63s23p5 արգոն 18 1s632s
Ինչպե՞ս եք գրում MN-ի էլեկտրոնային կոնֆիգուրացիան:

Մյուս կողմից, մանգանն ունի 1s22s22p63s23p64s23d5 էլեկտրոնային կոնֆիգուրացիա և [Ar]4s23d5 ազնիվ գազի կոնֆիգուրացիա, ինչը հանգեցնում է մեկ չզույգված էլեկտրոնի յուրաքանչյուր 3d ենթաօրբիտալում։
