
- Հեղինակ Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- Վերջին փոփոխված 2025-01-22 17:01.
Նիլս Բորը բացատրեց որ գծային սպեկտր ջրածնի ատոմ ենթադրելով, որ էլեկտրոնը շարժվում է շրջանաձև ուղեծրերով և թույլատրվում է միայն որոշակի շառավղով ուղեծրեր։ Միջուկին ամենամոտ ուղեծիրը ներկայացնում էր միջուկի հիմնական վիճակը ատոմ և ամենակայունն էր. Ավելի հեռու ուղեծրերը ավելի բարձր էներգիայով գրգռված վիճակներ էին:
Նմանապես, ի՞նչ է բացատրում Բորի մոդելը:
Այն Բորի մոդելը ցույց է տալիս, որ ատոմներում էլեկտրոնները գտնվում են միջուկի շուրջ տարբեր էներգիայի ուղեծրերում (պատկերացրե՛ք Արեգակի շուրջ պտտվող մոլորակները): Բոր օգտագործել է էներգիայի մակարդակներ (կամ պատյաններ) տերմինը՝ տարբեր էներգիայի այս ուղեծրերը նկարագրելու համար:
Ավելին, ինչպե՞ս եք կարդում Բորի մոդելը:
- Նկարի՛ր միջուկը։
- Գրի՛ր միջուկում նեյտրոնների և պրոտոնների քանակը։
- Նկարեք առաջին էներգիայի մակարդակը:
- Էներգետիկ մակարդակներում գծե՛ք էլեկտրոնները ստորև նշված կանոնների համաձայն:
- Հետևեք, թե քանի էլեկտրոն է դրված յուրաքանչյուր մակարդակում և էլեկտրոնների քանակը, որոնք մնացել են օգտագործելու համար:
Նմանապես, կարելի է հարցնել, թե ինչպես են արտադրվում ատոմային սպեկտրները:
Երբ ատոմներ հուզված են, նրանք արձակում են որոշակի ալիքի երկարության լույս, որը համապատասխանում է տարբեր գույների: Արտանետվող լույսը կարելի է դիտարկել որպես գունավոր գծերի շարք, որոնց միջև կան մուգ բացատներ. գունավոր գծերի այս շարքը կոչվում է գիծ կամ ատոմային սպեկտրներ . Յուրաքանչյուր տարր արտադրում է եզակի հավաքածու սպեկտրալ տողեր.
Ի՞նչ եզրակացություն է արել Բորն իր մոդելում ջրածնի գծային սպեկտրը բացատրելու համար:
Բացատրություն: Բոր այս ենթադրությունը հիմնավորեց այն փաստի վրա, որ կան միայն մի քանիսը տողեր մեջ սպեկտրը որ ջրածինը ատոմը և նա հավատում էր, որ տողեր լույսի արձակման կամ կլանման արդյունք էին, երբ էլեկտրոնը մի ուղեծրից մյուսը տեղափոխվեց ատոմում:
Խորհուրդ ենք տալիս:
Ի՞նչ է Նիլ Բորի ատոմային մոդելը:

Նիլս Բորն առաջարկել է ատոմի Բորի մոդելը 1915 թվականին: Բորի մոդելը մոլորակային մոդել է, որտեղ բացասական լիցքավորված էլեկտրոնները պտտվում են փոքր, դրական լիցքավորված միջուկի շուրջ, որը նման է արևի շուրջ պտտվող մոլորակներին (բացառությամբ, որ ուղեծրերը հարթ չեն):
Ինչպե՞ս են արտանետումների սպեկտրները վկայում Բորի մոդելի էլեկտրոնային թաղանթների մասին:

Ատոմային սպեկտրներում միայն որոշակի գծերի առկայությունը նշանակում էր, որ էլեկտրոնը կարող է ընդունել միայն որոշակի դիսկրետ էներգիայի մակարդակներ (էներգիան քվանտացված է); այստեղից էլ առաջացել է քվանտային թաղանթների գաղափարը: Ատոմի կողմից կլանված կամ արտանետվող ֆոտոնների հաճախականությունները ամրագրված են ուղեծրի էներգիայի մակարդակների տարբերություններով
Ինչո՞վ է Շրոդինգերի մոդելը տարբերվում Բորի մոդելից:

Բորի մոդելում էլեկտրոնը դիտարկվում է որպես միջուկի շուրջ ֆիքսված ուղեծրերի մեջ գտնվող մասնիկ: Շրոդինգերի մոդելը (Քվանտային մեխանիկական մոդել) թույլ տվեց էլեկտրոնին զբաղեցնել եռաչափ տարածություն։ Հետևաբար, ատոմում էլեկտրոնների բաշխումը նկարագրելու համար պահանջվում էր երեք կոորդինատ կամ երեք քվանտային թիվ
Ինչպե՞ս եք հաշվարկում բորի ատոմային զանգվածը:
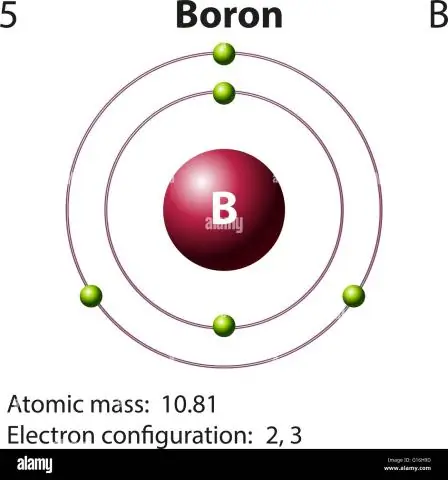
Բորի համար այս հավասարումը կունենա հետևյալ տեսքը. 5 պրոտոն + 5 նեյտրոն = 10 ատոմային զանգվածի միավոր (AMU) կամ ավելի հաճախ հանդիպող բորի իզոտոպի համար (մոտ 5 պրոտոն + 6 նեյտրոն = 11 AMU):
Ինչպե՞ս է փարոսի մոդելը բացատրում պուլսարները:

Պուլսարները բացատրում է որպես պտտվող նեյտրոնային աստղեր, որոնք ճառագայթման ճառագայթներ են արձակում իրենց մագնիսական բևեռներից։ Երբ նրանք պտտվում են, նրանք փարոսների պես ավլում են երկնքի ճառագայթները. եթե ճառագայթներն անցնում են Երկրի վրայով, աստղագետները հայտնաբերում են իմպուլսներ: Երբ գերնոր աստղը պայթում է, միջուկը շատ փոքր չափերի է փլուզվում
